 Aux États-Unis, le scandale fait rage, en France,
personne ne bronche. L'affaire pourrait pourtant ravaler le Médiator au rang de
simple pastille Valda...
Aux États-Unis, le scandale fait rage, en France,
personne ne bronche. L'affaire pourrait pourtant ravaler le Médiator au rang de
simple pastille Valda...
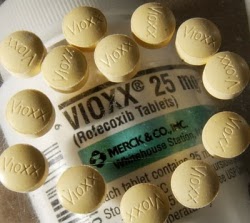
Le Médiator a tué 2000 personnes. Scandale ! Que penser, alors, du Vioxx, ce médicament anti-douleur et anti-inflammatoire largement utilisé contre l'arthrite entre 1999 et 2004. Il aurait, selon la FDA (Food and Drug Administration, agence de régulation américaine des médicaments) provoqué 160 000 crises cardiaques et attaques cérébrales et 30 000 décès, rien qu'aux États-Unis. Chiffre récemment réévalué à 40 000 par une nouvelle étude. En France, c'est le flou artistique... y a-t-il eu un seul mort ? On ne le saura peut-être jamais...
Cœurs sensibles s'abstenir
En 2007, le géant pharmaceutique Merck (commercialisant le Vioxx) a négocié un règlement à l'amiable concernant 95% des 26.600 plaintes déposées contre lui, pour un montant de 5 milliards de dollars. Mais certains plaignants ont refusé l'arrangement, et les procès qui suivent leur cours dévoilent régulièrement quelques cadavres, bien planqués au fond des placards. Le bimensuel Archives of Internal Medicine a notamment révélé, l'année dernière, que Merck n'avait pas publié les résultats d'études cliniques effectuées après la mise sur le marché du médicament. Un oubli, sans doute. Fâcheux, puisque ces études montraient dès 2001 que le Vioxx augmentait nettement le risque d'attaques cardiaques et cérébrales. Un accroissement estimé à 35% en juin 2001, à 39% en avril 2002 et à 43% en septembre 2004, au moment de son retrait du marché. Malgré ces études, le laboratoire a toujours nié tout risque sanitaire... et pendant ce temps là, il continuait d'accumuler les profits, 2 milliards de dollars tous les ans.
L'Afssaps en double aveugle
Dans cette affaire, les autorités sanitaires, dont l'Agence française de sécurité des produits sanitaires (Afssaps), ont été d'une passivité exemplaire. En novembre 2000, l'étude américaine Vigor prouve que le Vioxx entraine une très nette augmentation du nombre d'infarctus du myocarde, ce qu'admet l'Afssaps dans un communiqué. Mais notre Agence nationale fait valoir qu'à l'origine, cette étude n'avait pas "pour objectif l'étude de la tolérance cardio-vasculaire", elle ne vaudrait donc pas grand chose car "seule une étude spécifique permettrait d'évaluer le risque cardio-vasculaire éventuel" du médicament. Et les patients sont priés de gober la pilule.
En juin 2002, constatant que le Vioxx est devenu un best-seller en quelques mois (Merk a cartonné sur la pub'), le coeur léger, l'Afssaps se décide tout même à recommander aux médecins d'avoir la main un peu plus légère sur les prescriptions, car la molécule engendrerait des effets secondaires notables... sur le système digestif. Quand aux risques cardio-vasculaires, il "est en cours d'évaluation". En juillet 2004, l'Afssaps rend compte d'une réévaluation du rapport bénéfice/risque avalisée par la Commission européenne quatre mois plus tôt : RAS, tout va bien, "la sécurité d'emploi des coxibs [dont le Vioxx fait partie] n'est pas remise en cause". Et bonjour chez vous.
C'est alors qu'en septembre 2004, l'Agence tombe des nues. Elle annonce, dans un communiqué, qu'elle "vient d'être informée [...] de la décision des laboratoires Merck Sharp & Dohme-Chibret de l'arrêt mondial de la commercialisation de leur spécialité Vioxx". Il lui faudra 9 mois de plus pour admettre officiellement que le médicament est effectivement dangereux sur le plan cardio-vasculaire. Ce que ne contesteront certainement pas les milliers de malheureux qui ont claqué entre temps...
Ce qu'on appelle un plan (de pharmacovigilance) qui se déroule sans accro(c)... ?
Tiré d’un article http://www.lesmotsontunsens.com